Les thérapies ciblées s'attaquent aux cancers pédiatriques

Les traitements des cancers pédiatriques ont nettement progressé et aujourd’hui, près de 80 % peuvent être guéris. Mais pour les 20 % restants, d’autres options sont nécessaires. Lors du congrès de l’ASCO 2019, plusieurs études confirment l’intérêt des thérapies ciblées pour ces cancers réfractaires, et en particulier d’une nouvelle classe de médicament : les inhibiteurs de TRK.
Faciliter l’accès à des thérapies ciblées pour les cancers pédiatriques
Face au cancer, les thérapies ciblées permettent de bloquer un mécanisme de croissance propre à certaines cellules cancéreuses. Une fois les patients sélectionnés (leur tumeur présentant cette particularité à cibler), l’action thérapeutique est efficace et moins toxique. Aujourd’hui, cette démarche largement intégrée à la prise en charge du cancer chez l’adulte (pour le cancer du sein, du poumon, du côlon…) mais pas chez l’enfant car peu de ces médicaments ont été autorisés en pédiatrie.
Mais aujourd’hui en Europe et aux Etats-Unis, les cancers pédiatriques ne répondant pas aux traitements conventionnels ou aux cancers de mauvais pronostic font l’objet de recherches cliniques permettant de savoir si ces tumeurs peuvent bénéficier de traitements éprouvés chez l’adulte.
160 gènes testés, 10 thérapies ciblées disponibles…
Présentée lors du congrès de l’ASCO 2019, l’étude américaine Pediatric MATCH s’adresse aux enfants atteints d’un cancer qui n’a pas répondu aux traitements standard. Elle prévoit de rechercher les altérations génétiques spécifiques des tumeurs de chaque patient, de leur offrir les médicaments ciblant les altérations retrouvées (quel que soit le type de cancer) et d’évaluer l'impact des traitements. Au total, 10 thérapies ciblées différentes1 sont accessibles dans le cadre de cet essai MATCH.
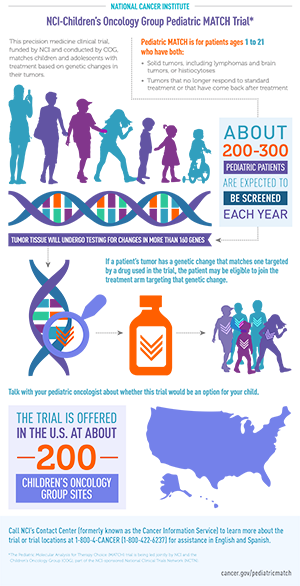
Fin de 2018, l’étude2 portait sur 422 enfants, adolescents et jeunes adultes : 101 patients (24%) atteints de tumeurs cérébrales, 300 (71%) atteints d'autres tumeurs solides et 21 (5%) atteints de lymphomes ou de troubles histiocytaires (des troubles rares affectant le système immunitaire). Alors que le séquençage des tumeurs (ADN et ARN sur plus de 160 gènes) était terminé pour 357 patients (92%), des "altérations génétiques ciblables" ont été identifiées chez 112 patients (29 %), dont 95 (24 %) ont pu recevoir l’un des 10 traitements disponibles3. À la fin de 2018, 39 patients (10%) avaient participé à un essai clinique de traitement du MATCH en pédiatrie, d'autres patients appariés étant toujours éligibles pour un traitement à une date ultérieure4. A terme, l’étude Pediatric MATCH doit recruter au moins 1 000 patients et inclure de nouvelles thérapies ciblées (et des immunothérapies) afin d'augmenter encore le nombre de patients pouvant bénéficier d’un traitement.
MappyActs : le larotrectinib, première thérapie ciblée des tumeurs solides de l’enfant ?
En Europe, l’essai MappyActs piloté par Gustave Roussy s’adresse aux tumeurs pédiatriques réfractaires ou en récidive. Toutes les tumeurs font l’objet d’un prélèvement et d’une analyse génétique permettant d’identifier des traitements potentiels. Présentés dans le cadre de l’ASCO 2019, des résultats5 a montré l’intérêt d’une nouvelle classe de médicament pour ces tumeurs : les inhibiteurs des protéines de fusion TRK (tropomyosin receptor kinase) capables de bloquer sélectivement ces anomalies génétiques intervenant dans de nombreux types de cancers. Elles surviennent au début du développement du cancer et restent présentes jusqu’à sa dissémination le cas échéant. Elles agissent en envoyant des signaux visant à stimuler la croissance des cellules cancéreuses.
L’un de ces médicaments, le larotrectinib a été testé sur 34 enfants atteints de cancers réfractaires présentant cette anomalie. Les résultats très préliminaires montrent que 94% ont vu leur maladie se stabiliser ou régresser (taux de réponse).
Le larotrectinib a été autorisé aux Etats-Unis pour toutes les tumeurs adultes et pédiatriques présentant des fusions TRK, sans précision sur l’origine du cancer (on parle ainsi d’une indication dite "agnostique" non dépendante d’un type de tumeur mais liée à une altération génétique). L’Agence Européenne du Médicament étudie actuellement le dossier. En France, dans l’attente de son AMM, ce médicament bénéficie d’une autorisation temporaire d’Utilisation de cohorte depuis quelques semaines.
L’entrectinib, une arme multicible pour des cancers pédiatriques
Une autre étude6 portant sur un composé original, l’entrectinib a donné des résultats encore plus encourageants. Ce médicament est capable d’inhiber plusieurs voies de croissance des cellules cancéreuses liées aux mutations des gènes NTRK1/2/3, mais aussi ROS1 et ALK. Il se distingue des autres médicaments de la même classe car il cible plusieurs mutations et parce qu’il est capable de passer la barrière hémato-encéphalique pour pénétrer dans le système nerveux central.
Présentée lors du congrès de l’ASCO 2019, une étude a été conduite sur 29 patients âgés de 4,9 mois à 20 ans (âge moyen de 7 ans), qui avaient soit une tumeur du système nerveux central, soit un neuroblastome, soit une autre tumeur solide, dont 12 avaient une des mutations ciblées par ce médicament. Résultat : 100% des patients présentant les mutations ciblées ont répondu à l'entrectinib (tumeur réduite ou disparue). Aucune réponse n'a été observée chez les patients ne présentant pas les altérations ciblées par l'entrectinib.
En fonction des tumeurs des patients portant les mutations ciblées, les résultats ont été :
- Pour les tumeurs du système nerveux central : Parmi les cinq patients présentant des tumeurs évaluables du SNC, tous ont eu une réponse objective - un a eu une réponse complète (disparition de la tumeur) et 4 une réponse partielle (réduction de plus de 50 % de la tumeur). Le patient restant n'a pas encore été évalué.
- Tumeurs extra-crâniennes : Six patients atteints de tumeurs solide en dehors du système nerveux central ont présenté une réponse objective au traitement : un patient a vu la tumeur disparaître et 5 une réponse partielle (réduction de 30% ou plus de la maladie).
- Neuroblastome : Un patient a eu une réponse complète.
Tous ces résultats démontrent l’intérêt de ces médicaments pour les cancers pédiatriques et l'utilité du d’un diagnostic moléculaire des tumeurs chez les enfants, quel que soit leur âge. Cette disposition est inscrite en France dans le Plan France Médecine Génomique 2025 (projets Sequoia et Auragen).
1 - Les traitements, dont beaucoup sont testés chez les enfants pour la première fois, comprenaient : le larotrectinib, l’erdafitinib ciblant FGFR, tazemetostat ciblant EZH2 et d'autres gènes du complexe SWI / SNF, LY3023414- ciblant la voie PI3K / MTOR, sélumétinib - ciblant la voie MAPK, ensartinib- ciblant ALK ou ROS1, vemurafenib- ciblant BRAF, olaparib ciblant les défauts de réparation des dommages de l'ADN, le palbociclib, ulixertinib- ciblant la voie MAPK
2 - Abstract 10011: Identification of targetable molecular alterations in the NCI -COG Pediatric MATCH trial - Donald Williams Parsons et al. – ASCO 2019 (accessible en ligne)
3 - Plus largement, des "altérations ciblables" ont été détectées chez plus de 40 % des enfants atteints de tumeurs cérébrales et chez plus de 25 % des enfants pour les autres types de cancer testés : le plus souvent des mutations du gène RAS , retrouvées chez 16 patients; Mutations ou fusions de BRAF , retrouvées chez 14 patients; Mutations ou délétions SMARCB1 , retrouvées chez 14 patients; Mutations de NF1 , retrouvées chez 11 patients; et de nombreuses modifications survenant chez moins de 10 patients chacune.
4 - Les chercheurs ont également collecté des échantillons de sang qui seront également séquencés, afin de déterminer si certaines mutations peuvent relever d’un caractère héréditaire. Dans ce cas, une information et une évaluation génétique pour le patient et sa famille seront mis en place.
5 - Larotrectinib efficacy and safety in pediatric TRK fusion cancer patients - Cornelis Martinus van Tilburg et al. - J Clin Oncol 37, 2019 (suppl; abstr 10010) (accessible en ligne)
6 - Phase 1/1B trial to assess the activity of entrectinib in children and adolescents with recurrent or refractory solid tumors including central nervous system (CNS) tumors - Giles W. Robinson et al. - J Clin Oncol 37, 2019 (suppl; abstr 10009) (accessible en ligne)








