Cancer de la vessie avancé : l'immunothérapie change la donne


Détecté tardivement, le cancer de la vessie est particulièrement redoutable, avec peu d’options thérapeutiques. Depuis plus de 30 ans, son traitement repose sur une chimiothérapie particulièrement toxique, difficile à administrer chez une population âgée. Mais l’arrivée d’une immunothérapie, l’atezolizumab (Tecentriq ®) apporte des résultats qui lui ont valu, aux Etats-Unis, son autorisation de mise sur le marché, le 7 juin 2016.
Deuxième cause de cancers urologique, le cancer de la vessie touche préférentiellement les hommes. On compte chaque année près de 10 000 nouveaux cas en France et 3 000 décès liés à ce type de cancer. Le principal facteur de risque est le tabac. Cette tumeur se développe à partir des cellules de la paroi de la vessie. On parle le plus souvent de carcinomes urothéliaux.
Cancer de la vessie : peu de solutions pour les formes avancées
Plus il est détecté tôt mieux il est traité1.
- Dans 70 à 80 % des cas, la tumeur est superficielle et strictement localisée sur la muqueuse urothéliale. La chirurgie consistant à une ablation par résection transurétrale de la vessie est préconisée. Après opération, un traitement par chimiothérapie est appliqué dans la vessie. En cas de risque élevé de récidive ou de progression, un traitement d’immunothérapie (BCG), associée à la chimiothérapie est également administré directement dans la vessie. Une ablation de la vessie est envisagée dans certains cas de risque élevé de récidive ou de progression ou en cas d’échec au traitement par BCG.
- Pour les cas plus évolués, la tumeur a envahi la muqueuse urothéliale jusqu’au muscle de la vessie. La chirurgie précédée d’une chimiothérapie (néoadjuvante) est le traitement de référence et consiste en l’ablation de la vessie et des ganglions à proximité. Parfois, la chimiothérapie ne sera prescrite qu’après chirurgie (chimiothérapie adjuvante). En cas d’ablation de la vessie, une néovessie (construite à partir de l’intestin grêle) ou une stomie (dérivation urinaire vers une poche externe) est mise en place. La surveillance se fait ensuite tous les trois mois.
- En cas d’évolution vers une forme métastatique ou un diagnostic d’emblée métastatique (le cancer s’est propagé vers d’autres organes), les options thérapeutiques sont jusqu’alors très réduites. La chirurgie n’est plus possible et l’essentiel de la prise en charge vise à contrôler autant que possible la maladie par la chimiothérapie… lorsque cette dernière peut être administrée malgré sa forte toxicité.
Mais face aux formes les plus avancées, les plus difficiles à traiter, de nouvelles immunothérapies apportent des résultats étonnants.
Tecentriq ®, l’anti-PD-L1 qui change le traitement du cancer de la vessie avancé
Face aux cellules cancéreuses, les lymphocytes T (les globules blancs qui aident aussi à lutter contre les infections) sont mobilisés, mais la tumeur va se mettre à exprimer à sa surface une molécule appelé PD-L1. Cette molécule va interagir avec une autre qui se trouve à la surface des lymphocytes appelée PD-1. Et la rencontre des deux va rendre l'armée des lymphocytes T totalement inefficace. L’enjeu thérapeutique est donc d’empêcher cette liaison en bloquant PD-1 ou PD-L1.
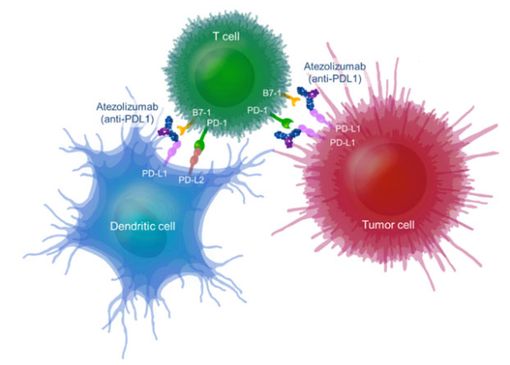
Développé par Roche, l’atezolizumab (Tecentriq ®) dont nous vous parlions dès 2014, est un anticorps monoclonal conçu pour se lier directement à une protéine appelée PD-L1 exprimé sur les cellules tumorales et les cellules immunitaires infiltrant les tumeurs2. En bloquant la voie PD1/PD-L1, le médicament permet ainsi l’activation des lymphocytes T, le système immunitaire peut s’attaquer à la tumeur. Certaines tumeurs expriment plus que d’autres PD-L1 à leur surface, ce pourcentage d’expression pourrait constituer un indicateur d’efficacité du Tecentriq ® (mais également des autres immunothérapies ciblant la voie PD1/PD-L1).
L’immunothérapie nouvelle arme contre les cancers de la vessie
Ce médicament fait l’objet d’une étude face au cancer de la vessie localement avancé ou métastatique. Deux groupes ont été distingués :
- Les patients qui dont la maladie a progressé pendant ou après une chimiothérapie à base de platine, donnée avant (traitement néoadjuvant) ou après la chirurgie (traitement adjuvant)
- Les patients qui n’ont pas pu recevoir cette chimiothérapie jugée trop toxique pour eux. Près de la moitié des patients atteints d’un cancer de la vessie avancé sont trop fragiles pour recevoir une chimiothérapie à base de cisplatine. Pour eux, il n’existe pas jusqu’alors de traitement éprouvé.

Les résultats pour le premier groupe ont valu à Roche une homologation accélérée de ce médicament dans cette indication par la Food and Drug Administration, l’agence du médicament américaine3. Après 14,4 mois de suivi, 14,8 % de l’ensemble des patients ont connu une régression de leur tumeur, avec une durée de la réponse au traitement qui atteignait 12,7 mois chez les patients dont la tumeur exprimait peu PD-L1 et qui perdurait au-delà de la durée de suivi pour les patients dont la tumeur exprimait PD-L1.
Les résultats pour le second groupe4 ont été présentés lors du congrès de l’ASCO 2016. Après un suivi de 14,4 mois, 24 % des patients ont répondu au traitement (7 % ont connu une réponse complète). La plus longue durée de la réponse a dépassé 18 mois et chez 75 % des répondeurs, la réponse perdurait au moment de l’analyse des données. La médiane de survie était de 14,8 mois. Dans cet essai, la toxicité du Tecentriq ® était faible, avec 10-15% des patients connaissant des effets secondaires sévères (hypothyroïdisme, problèmes hépatiques, cutanés, diarrhée…). Seuls 6 % des patients ont arrêté le traitement à cause d’un effet secondaire, bien moins qu’avec une chimiothérapie pour des patients âgés.
Enfin, une troisième étude multicentrique conduite sur 300 patients ayant un cancer de la vessie localement avancé ou métastatique et ne répondant pas à une chimiothérapie à base de platine, montrent que 20 % des patients ont une réponse à l’atezolizumab. Le taux de survie globale est de 8 mois, avec plus d’un tiers des patients en vie à un an. Par ailleurs, dans un sous-groupe de patients, la survie atteint pratiquement 12 mois, soit le double qu’avec une chimiothérapie classique. Les résultats de cette étude ont été publiés dans la revue Lancet Oncology5.
Tecentriq®: feu vert aux Etats-Unis
A la lumière de ces résultats, l’atezolizumab Tecentriq ® a reçu, son autorisation de mise sur le marché aux Etats-Unis le 7 juin 20166, soit dès le lendemain de la présentation des résultats des études présentés à l'ASCO, la veille.
Tecentriq ® fait l’objet d’un développement dans de nombreuses indications en monothérapie dans le cancer du poumon, en association avec des thérapies ciblées dans le cancer colorectal, le cancer du sein triple négatif…
1 - Pour en savoir plus, l’Institut national du cancer propose un tableau des traitements en fonction des différents stades de la maladie.
2 - En ciblant PD-L1 qui est sur la tumeur, le laboratoire Roche espère que la toxicité de son composé sera moins importante qu’en ciblant PD-1 au niveau des lymphocytes T, comme pour le pembrolizumab (Keytruda ®).
3 - FDA approves new, targeted treatment for bladder cancer – communiqué de presse de la FDA 18 mai 2016 (accessible en ligne)
4 - Atezolizumab (atezo) as first-line (1L) therapy in cisplatin-ineligible locally advanced/metastatic urothelial carcinoma (mUC): Primary analysis of IMvigor210 cohort 1 - Arjun Vasant Balar et al. - J Clin Oncol 34, 2016 (suppl; abstr LBA4500) (abstract accessible en ligne)
5. Rosenberg JE, Hoffman-Censits J, Powels T, van der Heijden MS et al. Atezoizumab in patients with locally advanced and metastatic urothelial carcinoma who have progressed following treatment with platinum-based chemotherapy: a single-arm, multicentre phase 2 trial.The Lancet Oncology May 2016; 37. No 10031:1909-20 (article en ligne).
6. National Cancer Institute. FDA approves new immunotherapy drug for bladder cancer. June 7 2016 (document en ligne).









